Biochimica e chimica organica
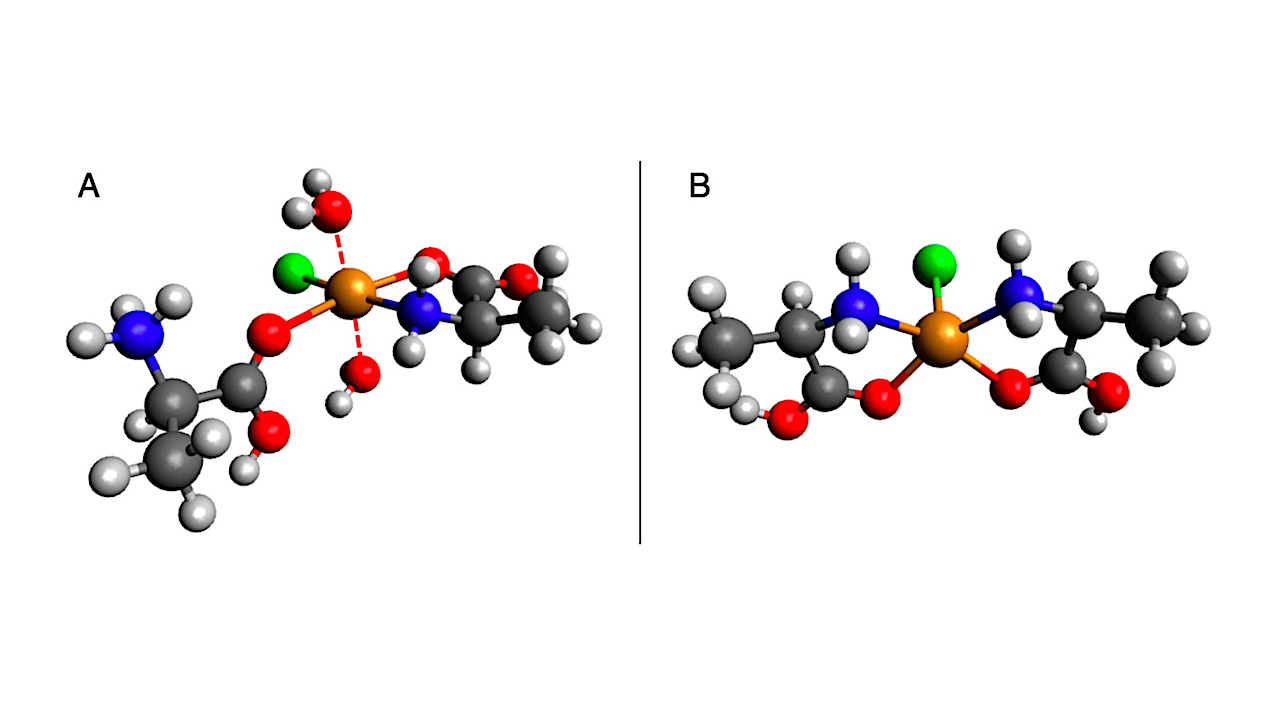
(A) Il complesso attivo proposto da Rudd et al. (1990) per la reazione SIPF di una molecola di alanina protonata e neutra [18]. (b) Un altro composto attivo di SIPF tra due molecole neutre di alanina in una configurazione cis come proposto da Rimola et al. (2007) [20]. Qui, cis si riferisce alla posizione relativa degli atomi di N (o equivalente O) sullo stesso lato del piano contenente l’atomo di rame. In questa figura, il rosso rappresenta l’ossigeno, il blu rappresenta l’azoto, il grigio rappresenta il carbonio, il grigio chiaro rappresenta l’idrogeno, l’arancione rappresenta il rame e il verde rappresenta il cloro. – vita
La reazione di formazione del peptide indotta dal sale (SIPF) è un meccanismo biologicamente plausibile per la polimerizzazione spontanea degli amminoacidi in peptidi sulla Terra primordiale.
Indagini sperimentali sulla reattività del SIPF hanno scoperto che, in determinate condizioni, l’enantiomero le è più reattivo dell’enantiomero d, indicando il suo potenziale ruolo nell’emergenza del biocongenere. Un lavoro precedente aveva ipotizzato che la distorsione del complesso CuCl attivo verso una struttura simile al tetraedro aumenta l’asimmetria centrale sullo ione rame, che amplifica le differenze energetiche intrinseche che violano la valenza tra gli enantiomeri degli amminoacidi l e d, portando alla stereoselettività. Le valutazioni computazionali di questa teoria sono state limitate alle forme l + l protonate neutre del composto attivo CuCl.
Qui, i metodi della teoria del funzionale della densità sono stati utilizzati per confrontare le energie e le geometrie dei complessi di aminoacidi CuCl omogenei (l + l e d + d) ed eterogenei (l + d) per forme positive, neutre e neutre di alanina, valina, e prolina. Non sono state osservate differenze energetiche significative tra i diversi complessi attivi (cioè d + d, l + l vs. l + d) e le deformazioni dei complessi attivi tra i sistemi stereoselettivi e non stereoselettivi non erano coerenti, indicando che la geometria del complesso attivo non lo è. È il principale fattore della stereoselettività osservata della reazione SIPF.
Alison C. Fox, Jason D. Boettger, EL Berger e Aaron S. Burton
Vita 2023, 13(9), 1796; doi: 10.3390/life13091796
https://www.mdpi.com/2075-1729/13/9/1796
Astrobiologia

“Studioso di caffè. Appassionato di cibo. Appassionato di birra. Introverso. Praticante di Internet in modo irritante e umile.”







